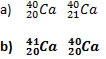VOLVER A LOS ARTÍCULOS
VOLVER A LOS ARTÍCULOS
EJERCICIOS
peso - volumen - color - punto de fusión - longitud - punto de ebullición - densidad - olor - sabor - temperatura
| Propiedades intensivas | Propiedades extensivas |
|---|---|
| |
|
a) Materia es todo aquello que tiene masa y ________________.
color - temperatura - volumen
b) Todos los cuerpos materiales están formados por unidades fundamentales llamadas ______________.
átomos - enlaces - sustancias
c) Los átomos, dependiendo de su naturaleza, pueden unirse entre sí formando ___________.
materia - enlaces - masa
d) La temperatura está directamente relacionada con la _____________ que tienen los átomos o partículas que componen los cuerpos.
presión - energía - masa
e) Las partículas de los ___________ se atraen muy poco entre sí y están separadas.
sólidos - líquidos - gases
f) Las partículas de los sólidos se atraen con ___________fuerza entre sí y están fuertemente unidas.
mucha - poca - intermedia
g) El estado de una sustancia depende de la naturaleza de la sustancia y _______________.
temperatura - masa - color
h) La _____________ de un cuerpo mide la cantidad de materia que este contiene.
densidad - masa - temperatura
i) A la división entre la masa y el volumen de un cuerpo se le llama _____________ (d = m/V).
peso - densidad - energía

a) Fusión b) Vaporización c) Condensación d) Sublimación
a) Solidificación b) Condensación c) Sublimación regresiva d) Fusión
Z = 12:
Z = 25:
Z = 34:
I) Número de neutrones. II) Número de neutrones menos su número de protones. III) Número de electrones.
a) Solo I
b) Solo II
c) Solo III
d) Solo II y III
a) Su número atómico es 8. b) Su número másico es 8. c) Su número atómico es 14. d) Su número másico es 14. e) Su número de electrones es 14.
H:
Na:
Ca:
O:
a) El electrón se encuentra en ______________.
b) El neutrón se encuentra en_______________.
d) El protón se encuentra en ________________.
| Elemento | Nombre | A | Z | Protones | Electrones | Neutrones | Metal/No metal/Gas inerte |
|---|---|---|---|---|---|---|---|
|
Na |
|||||||
|
Oxígeno |
|||||||
|
13 |
|||||||
|
12 |
|||||||
|
52 |
Metal |
||||||
|
5 |
6 |
||||||
|
19 |
|||||||
|
H |
Aniones:
Cationes:
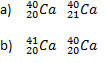
SOLUCIONES
peso - volumen - color - masa - punto de fusión - longitud - punto de ebullición - densidad - olor - sabor - temperatura
| Propiedades intensivas | Propiedades extensivas |
|---|---|
|
Punto de fusión Color Punto de ebullición Densidad Olor Sabor Temperatura |
Peso Volumen Longitud Masa |
a) Materia es todo aquello que tiene masa y volumen.
color - temperatura - volumen
b) Todos los cuerpos materiales están formados por unidades fundamentales llamadas átomos.
átomos - enlaces - sustancias
c) Los átomos, dependiendo de su naturaleza, pueden unirse entre sí formando enlaces.
materia - enlaces - masa
d) La temperatura está directamente relacionada con la energía que tienen los átomos o partículas que componen los cuerpos.
presión - energía - masa
e) Las partículas de los gases se atraen muy poco entre sí y están separadas.
sólidos - líquidos - gases
f) Las partículas de los sólidos se atraen con mucha fuerza entre sí y están fuertemente unidas.
mucha - poca - intermedia
g) El estado de una sustancia depende de la naturaleza de la sustancia y temperatura.
temperatura - masa - color
h) La masa de un cuerpo mide la cantidad de materia que este contiene.
densidad - masa - temperatura
i) A la división entre la masa y el volumen de un cuerpo se le llama densidad (d = m/V).
peso - densidad - energía
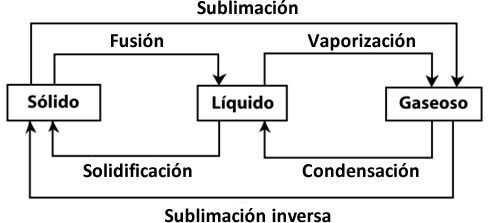
a) Fusión
b) Vaporización
c) Condensación
d) Sublimación
a) Solidificación
b) Condensación
c) Sublimación regresiva
d) Fusión
Z = 12: Magnesio
Z = 25: Manganeso
Z = 34: Selenio
I) Número de neutrones. II) Número de neutrones menos su número de protones. III) Número de electrones.
a) Solo I b) Solo II c) Solo III d) Solo II y III
a) Su número atómico es 8. b) Su número másico es 8. c) Su número atómico es 14. d) Su número másico es 14. e) Su número de electrones es 14.
H: 1s1
Na: 1s22s22p63s1
Ca: 1s22s22p63s23p64s2
O: 1s22s22p4
a) El electrón se encuentra en la corteza. b) El neutrón se encuentra en el núcleo. d) El protón se encuentra en el núcleo.
| Elemento | Nombre | A | Z | Protones | Electrones | Neutrones | Metal/No metal/Gas noble |
|---|---|---|---|---|---|---|---|
|
Na |
Sodio |
23 |
11 |
11 |
11 |
12 |
Metal |
|
O |
Oxígeno |
16 |
8 |
8 |
8 |
8 |
No metal |
|
Al |
Aluminio |
27 |
13 |
13 |
13 |
14 |
Metal |
|
Mg |
Magnesio |
24 |
12 |
12 |
12 |
12 |
Metal |
|
Cr |
Cromo |
52 |
24 |
24 |
24 |
28 |
Metal |
|
B |
Boro |
11 |
5 |
5 |
5 |
6 |
Metaloide |
|
K |
Potasio |
39 |
19 |
19 |
19 |
20 |
Metal |
|
Ar |
Argón |
40 |
18 |
18 |
18 |
22 |
Gas noble |
|
H |
Hidrógeno |
1 |
1 |
1 |
1 |
0 |
No metal |
Aniones: iones con carga neta negativa.
Cationes: iones con carga neta positiva.