 VOLVER A LOS ARTÍCULOS
VOLVER A LOS ARTÍCULOS
El método molar se basa en una serie de pasos para resolver los problemas estequiométricos según los datos que se faciliten:

Los problemas estequiométricos se clasifican según las siguientes relaciones:
A continuación se estudiarán los problemas tipo m-m, es decir, masa-masa. Estos problemas pueden ser de dos tipos: problemas con sustancias puras o problemas con sustancias impuras (se debe calcular el porcentaje de pureza). Tanto la sustancia conocida como la desconocida están en unidades de masa, en gramos.
Ejercicios:
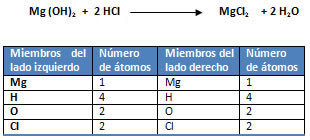
1. Un antiácido a base de leche magnesia Mg(OH)2 reacciona con el ácido clorhídrico HCl de los jugos gástricos de una persona con acidez. Calcular la cantidad de HCl neutralizado por 30 g de Mg(OH)2 y su rendimiento teórico.

mHCl= ¿? ; mMg(OH)2 = 30 gramos ; rendimiento teórico= ¿?
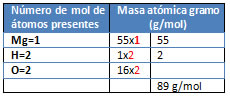
M= Mg(OH)2
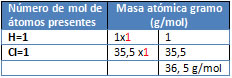
M= HCl
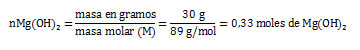

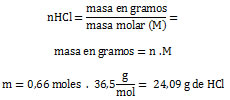
Referencias bibliográficas:
Ramos, F; Caballero, A (2000). Química teoría. 1er año Ciclo Diversificado. Ciencias y Ciclo Profesional. Caracas, Venezuela. Pág: 76-99.