 VOLVER A LOS ARTÍCULOS
VOLVER A LOS ARTÍCULOS
Los ácidos oxácidos u oxácidos son compuestos ternarios que resultan de un óxido ácido más agua, formulándose según las reglas de la I.U.P.A.C, con el elemento más electropositivo a la izquierda, el hidrógeno, seguido de un elemento central (no metal o un elemento de transición), y por último el elemento más electronegativo a la derecha, el oxígeno.
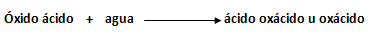
Según el sistema Stock, para ácidos oxácidos u oxácidos, se utilizan dos sistemas, el funcional y el sistemático, siguiendo la fórmula general: HiXiOi, donde H, es el hidrógeno, el X el no metal o elemento de transición, O, el oxígeno, e i el número de átomos de cada elemento en la fórmula. Estudiemos a continuación, la nomenclatura funcional Stock y sistemático Stock para los oxácidos:
1. Sistema funcional Stock:
Ácido + prefijo + oxo + raíz del nombre del átomo central + ico + (número de oxidación)
Estudiemos los siguientes ejemplos de oxácidos:
a) HClO4: esta fórmula corresponde al ácido tetraoxoclórico (VII). El prefijo tetra proviene del los cuatro átomos de oxígeno y el sufijo ico del cloro, el cual está utilizando el número de oxidación 7. Revisemos la sumatoria del producto entre los números de oxidación y subíndices de los elementos en la fórmula:
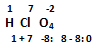
b) H2S2O7: esta fórmula corresponde ácido heptaoxodisulfúrico (VI). El prefijo griego hepta corresponde a los siete átomos de oxígeno y el prefijo di a los dos átomos de azufre, el cual está utilizando el número de oxidación 6. Cuando el elemento central se encuentra mayor a una unidad se indica con un prefijo griego luego de la palabra oxo. Revisemos la sumatoria del producto entre los números de oxidación y subíndices de los elementos en la fórmula:
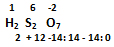
2. Nomenclatura sistemática Stock:
Prefijo + oxo + raíz del nombre del átomo central + ato + (número de oxidación) + de hidrógeno
Estudiemos los siguientes ejemplos de oxácidos:
a) HIO3: esta fórmula corresponde al trioxoiodato (V) de hidrógeno. El prefijo tri proviene de los tres átomos de oxígeno, la raíz iod correspondiente al elemento iodo (yodo), seguida del sufijo ato, elemento que está utilizando el número de oxidación 5. Revisemos la sumatoria del producto entre los números de oxidación y subíndices de los elementos en la fórmula:

b) H3AsO4: esta fórmula corresponde tetraoxoarseniato (V) de hidrógeno. El prefijo griego tetra corresponde a los cuatro átomos de oxígeno, la raíz arseni correspondiente al elemento arsénico, seguida del sufijo ato, elemento que está utilizando el número de oxidación 5. Revisemos la sumatoria del producto entre los números de oxidación y subíndices de los elementos en la fórmula:
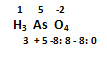
c) Cuando el número de átomos de oxígeno es mayor a 10, la I.U.P.A.C permite el uso del número arábigo en correspondencia, en lugar del prefijo griego. En el caso hipotético, siguiendo el ejemplo “b” si en lugar de los cuatro átomos de oxígeno tenemos once átomos, la nomenclatura sería, 11-oxoarseniato (V) de hidrógeno.
Nomenclatura tradicional o antigua:
La I.U.P.A.C recomienda el uso de las nomenclaturas Stock, sin embargo es necesario conocer la nomenclatura antigua o tradicional, tomando en cuanta que por lo estudiado, ambos tipos de nomenclatura requieren de un esfuerzo por el uso de prefijos y sufijos.
Para no metales con número de oxidación: 1, 3, 5, o 7 (cloro, bromo, yodo)

Estudiemos un ejemplo con el iodo (I): HIO, HIO2, HIO3, HIO4
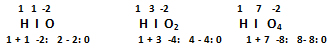
Orto: ácido oxácido de mayor hidratación.
Meta: ácido obtenido del orto por salida de una molécula de agua.
Piro: ácido obtenido por salida de una molécula de agua de dos moléculas de orto.

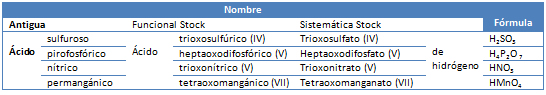
Las tres nomenclaturas descritas pueden compararse al estudiar la siguiente tabla con diferentes hidróxidos o bases.
Tabla 1. Comparación de nomenclaturas utilizadas para hidróxidos.
Referencias bibliográficas:
Cuerpo de redacción (1997). Mentor interactivo. Enciclopedia temática estudiantil. Editorial Océano. Barcelona, España. Pág: 411.
Suarez, F (2011). Química teoría. 4to año de Educación media general. Editorial Romor. Caracas, Venezuela. Pág: 17 - 18.