Tras el diamante y el grafito, los fullerenos son una de las formas estables en las que podemos encontrar el carbono. Se trata de moléculas de gran tamaño, con formas geométricas de elevada simetría y con propiedades que aún intrigan a la comunidad científica. Su descubrimiento dio paso a otros relevantes, como los nanotubos y grafenos.
DESCUBRIMIENTO
La alotropía se refiere a las formas de un elemento químico con estructura diferente pero un mismo estado físico; por ejemplo, el oxígeno gaseoso (O2) y el ozono (O3) son alótropos del oxígeno. Hasta 1985 se conocían solo dos formas alotrópicas del carbono: el diamante y el grafito.
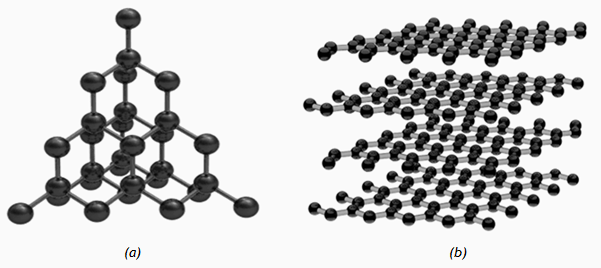
Fue entonces cuando los profesores de la Universidad Rice, Robert F. Curl y Richard E. Smalley; y Harold W. Kroto de la Universidad de Sussex develaron que la evaporación inducida por láser del grafito resultaba en una especie con fórmula molecular C60, la cual más tarde se llamó “buckminsterfullereno”.
El impacto científico y mediático de este descubrimiento hizo que la molécula C60 fuera nombrada “molécula del año” en 1991 según la revista Science y, además, concedió el premio Nobel en 1996 a Curl, Kroto y Smalley.
estructura de los fullerenos
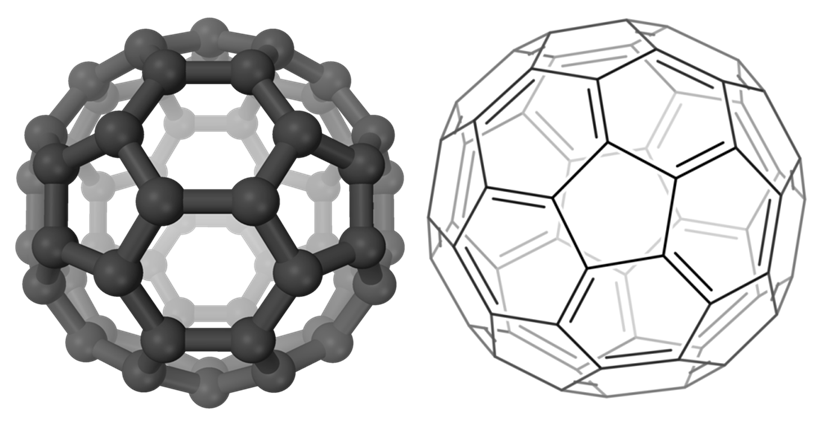
Los fullerenos son moléculas grandes con estructuras huecas compuestas exclusivamente por carbono y con una forma parecida a la de una esfera. Cada átomo de carbono está unido a otros tres (hibridación sp2) con enlaces desviados que le proporcionan cierta tensión que se distribuye por igual sobre toda la estructura gracias a la gran simetría de esta.
Geométricamente, la estructura cerrada de los fullerenos solo es posible si se combinan 12 anillos pentagonales y una cantidad de anillos hexagonales que puede variar.

C60: una molécula excepcional
La geometría icosaédrica del fullerenos C60 coincide con la de un balón de fútbol, sus propiedades más importantes son las siguientes:
- Tiene 120 operaciones de simetría, lo que la convierte en la molécula más simétrica.
- Es muy estable. Se necesitan más de 1.000 °C para destruirlo.
- Es muy electronegativa y forma con facilidad compuestos con átomos donadores de electrones.
- La molécula pura tiene una apariencia de polvo amarillo que se torna rosa al ser disuelto en disolventes definidos.
- Se polimerizan y forman enlaces entre esferas cercanas cuando se exponen a la luz ultravioleta intensa.
- Es fotosensible. Cambia sus propiedades al ser expuesta a la luz.
aplicaciones
Los fullerenos generan un gran interés en el sector científico, especialmente desde el punto de vista de la superconductividad. Algunas aplicaciones destacables son la catálisis, la fabricación de células solares, en telecomunicaciones, como recolectores de radicales libres y en pilas de combustible.
Gracias a sus propiedades ópticas, también se ha propuesto su uso en dispositivos fotónicos. Por otro lado, se estudia su uso como inhibidor de la proteasa del virus de inmunodeficiencia humana (VIH).




 VOLVER A LOS ARTÍCULOS
VOLVER A LOS ARTÍCULOS