Los alcanos pertenecen a los hidrocarburos, es decir, compuestos formados fundamentalmente por hidrógeno y carbono. Entre los hidrocarburos se pueden distinguir dos grandes grupos: los alifáticos y los aromáticos. Los alcanos conforman el primero de ellos, y son los compuestos orgánicos más sencillos.

Los hidrocarburos se clasifican en alifáticos y aromáticos. La diferencia principal entre estas categorías es que los alifáticos se conforman por cadenas abiertas y los aromáticos por cadenas cerradas o ciclos. Por ejemplo:
Butano, hidrocarburo alifático (de cadena abierta)
CH3-CH2-CH2-CH3
Ciclopentano, hidrocarburo aromático (de cadena cerrada)
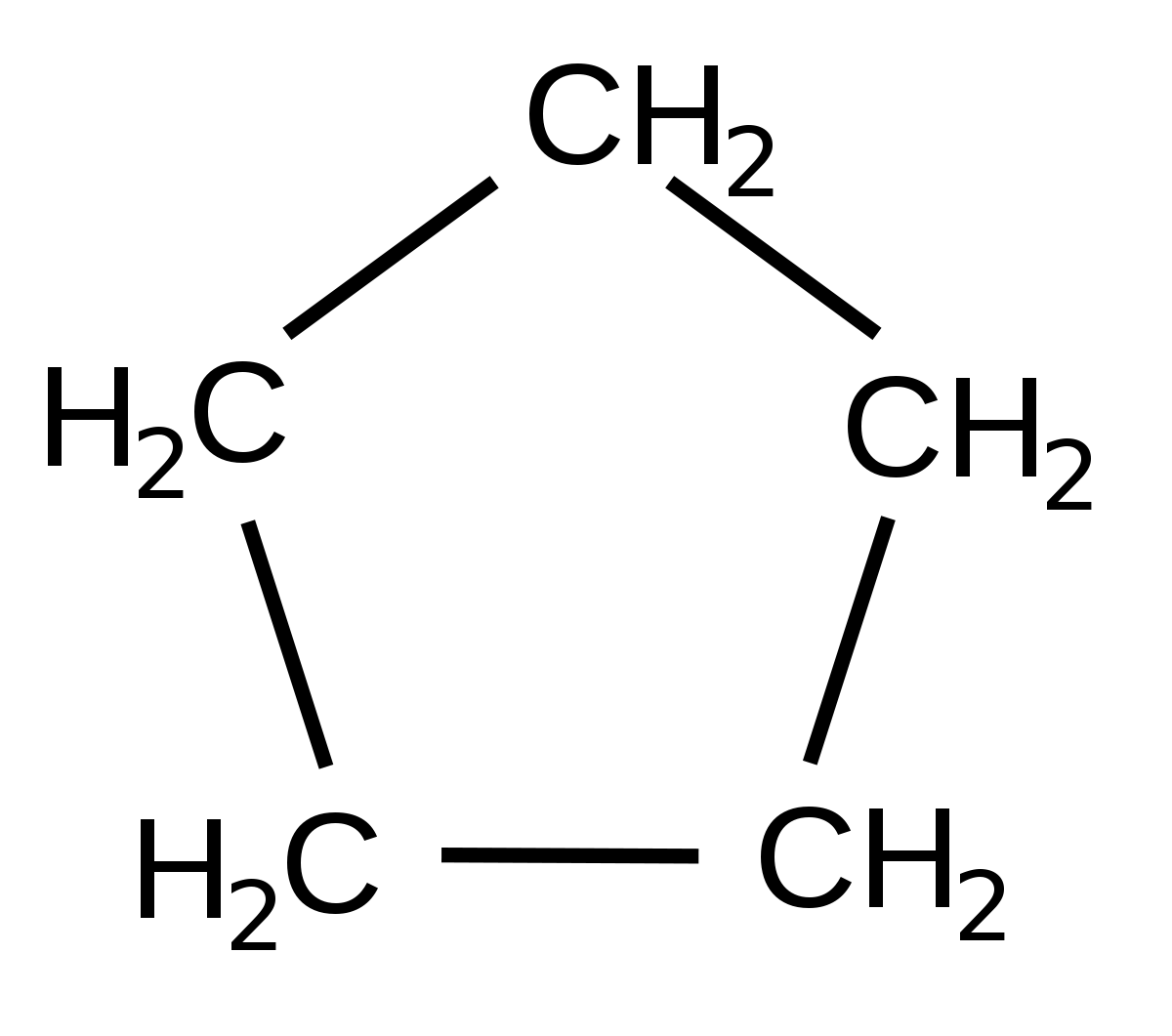
Entre los alifáticos se pueden encontrar los alcanos, alquenos y alquinos. Éstos, a su vez, se diferencian entre sí mediante la forma que tienen de unirse, es decir, por medio de los enlaces que los constituyen.
Alcanos: conformados por enlaces covalentes simples ( C-C ) de cadena abierta.
Alquenos: constituidos por enlaces covalentes dobles ( C=C ) de cadena abierta.
Alquinos: conformados por enlaces covalentes triples ( C≡C ) de cadena abierta.
ALCANOS

Los alcanos son considerados hidrocarburos saturados, ya que contienen únicamente enlaces simples en su estructura. Esta particularidad se debe a que los átomos de carbono que los conforman tienen una hibridación sp3, lo cual implica que contienen el numero máximo de átomos de hidrógeno que pueden unirse con los carbonos.
| HIBRIDACIÓN SP3
Para ejemplificar este tipo de hibridación es conveniente considerar la molécula del alcano más simple, el metano: CH4. El C tiene 4 electrones de valencia, por lo tanto, se puede representar el diagrama orbital de la siguiente forma:
Como se puede observar, existen dos electrones desapareados en los orbitales 2p2, con lo cual se podrían formar sólo dos enlaces con el hidrógeno. lo que originaría la especie CH2. Sin embargo, al excitar energéticamente a uno de los electrones del orbital sp2 se consigue obtener una especie más estable y la posibilidad de formar cuatro enlaces.
De este modo se obtienen los orbitales híbridos:
|
GEOMETRÍA MOLECULAR DEL METANO
 La hibridación implica también una reestructuración en la geometría molecular, en consecuencia, los orbitales sp3 apuntan hacia los vértices de un tetraedro regular. Todos los ángulos HCH miden 109,5°. Este tipo de hibridación no ocurre únicamente con alcanos, por ejemplo puede darse también en el amoníaco (NH3).
¿Qué otros tipos de hibridación se conocen?
Además de la hibridación sp3, se pueden obtener la sp y la sp2. Pero éstas no corresponden a alcanos.
|
NOMENCLATURA DE ALCANOS
Existen varias formas de representar a este tipo de compuestos, pero sea cual fuese la fórmula (molecular, desarrollada, semidesarrollada o taquigráfica) lo primero que se debe hacer es contar la cantidad de carbonos de la cadena principal. Para ello es de gran utilidad la siguiente tabla:
| N° de átomos de C | prefijo |
| 1 | met- |
| 2 | et- |
| 3 | prop- |
| 4 | but- |
| 5 | pent- |
| 6 | hex- |
| 7 | hept- |
| 8 | oct- |
| 9 | non- |
| 10 | dec- |
Tabla 1.
Fórmula desarrollada
Es aquella en la cual se pueden observar todos los átomos de la molécula con sus respectivos enlaces, por ejemplo:

Fórmula semidesarrollada
La fórmula semidesarrollada de un compuesto facilita su escritura, es una forma abreviada de la forma desarrollada.
El siguiente compuesto se denomina butano porque contiene 4 carbonos (ver tabla 1). La formula semidesarrollada se escribe teniendo en cuenta cuántos hidrógenos se encuentran alrededor de cada carbono.
A modo de ejemplo, se verá el caso del butano.

En los carbonos de los extremos de la cadena se observan uniones con tres hidrógenos, mientras que en los demás sólo hay capacidad para dos hidrógenos. Por lo tanto, la fórmula semidesarrollada es la siguiente:
CH3 – CH2 – CH2 – CH3
Formula molecular
Se conforma por símbolos químicos y subíndices que indican la cantidad total de cada uno de los elementos que constituyen el compuesto.
En los alcanos la fórmula general es Cn H2n+2, siendo n la cantidad total de carbonos existentes.
Por ejemplo, en el butano se encuentran 4 C, por lo tanto sería C4 H2.4+2= C4 H8+2 = C4H10

Fórmula taquigráfica
También denominada “fórmula de esqueleto” representa un par de átomos de carbonos unidos y se considera que tiene la cantidad de hidrógenos suficientes para completar los cuatro enlaces de carbono. Cada segmento cuenta con carbonos en sus extremos.

NOMENCLATURA DE ALCANOS LINEALES
La forma más utilizada es la semidesarrollada, el siguiente ejemplo paso a paso será de utilidad para aprender a nombrar alcanos lineales.
Nombrar el siguiente hidrocarburo:
a) CH3 – CH2 – CH2 – CH2 – CH3
Pasos a seguir:
- Contar la cantidad de átomos de C.
CH3 – CH2 – CH2 – CH2 – CH3
1 2 3 4 5
2. Buscar en la Tabla 1 el prefijo correspondiente.
| 4 | but- |
| 5 | pent- |
| 6 | hex- |
Como la cantidad de carbonos es de 5 átomos, el prefijo correspondiente es pent-
3. Se escribe el nombre iniciando con el prefijo que corresponde y finalizando de acuerdo a la cantidad de enlaces entre carbonos. En este caso son todos enlaces simples, por eso termina en “ano”.
CH3 – CH2 – CH2 – CH2 – CH3 PENTANO

A PRACTICAR LO APRENDIDO
1. Nombrar los siguientes alcanos lineales:
- CH3 – CH2 – CH3
- CH3 – CH2 – CH2 – CH2 – CH2 – CH2 – CH3
- CH3 – CH2 – CH2 – CH2 – CH2 – CH2 – CH2 – CH2 – CH3
2. Escribir las fórmulas semidesarrolladas de los siguientes alcanos:
- etano
- hexano
- octano
RESPUESTAS:
1. a. propano; b. heptano; c. nonano
2. a. CH3 – CH3
b. CH3 – CH2 – CH2 – CH2 – CH2 – CH3
c. CH3 – CH2 – CH2 – CH2 – CH2 – CH2 – CH2 – CH3
Para aprender más puedes ingresar a la Enciclopedia de Química.




 VOLVER A LOS ARTÍCULOS
VOLVER A LOS ARTÍCULOS

