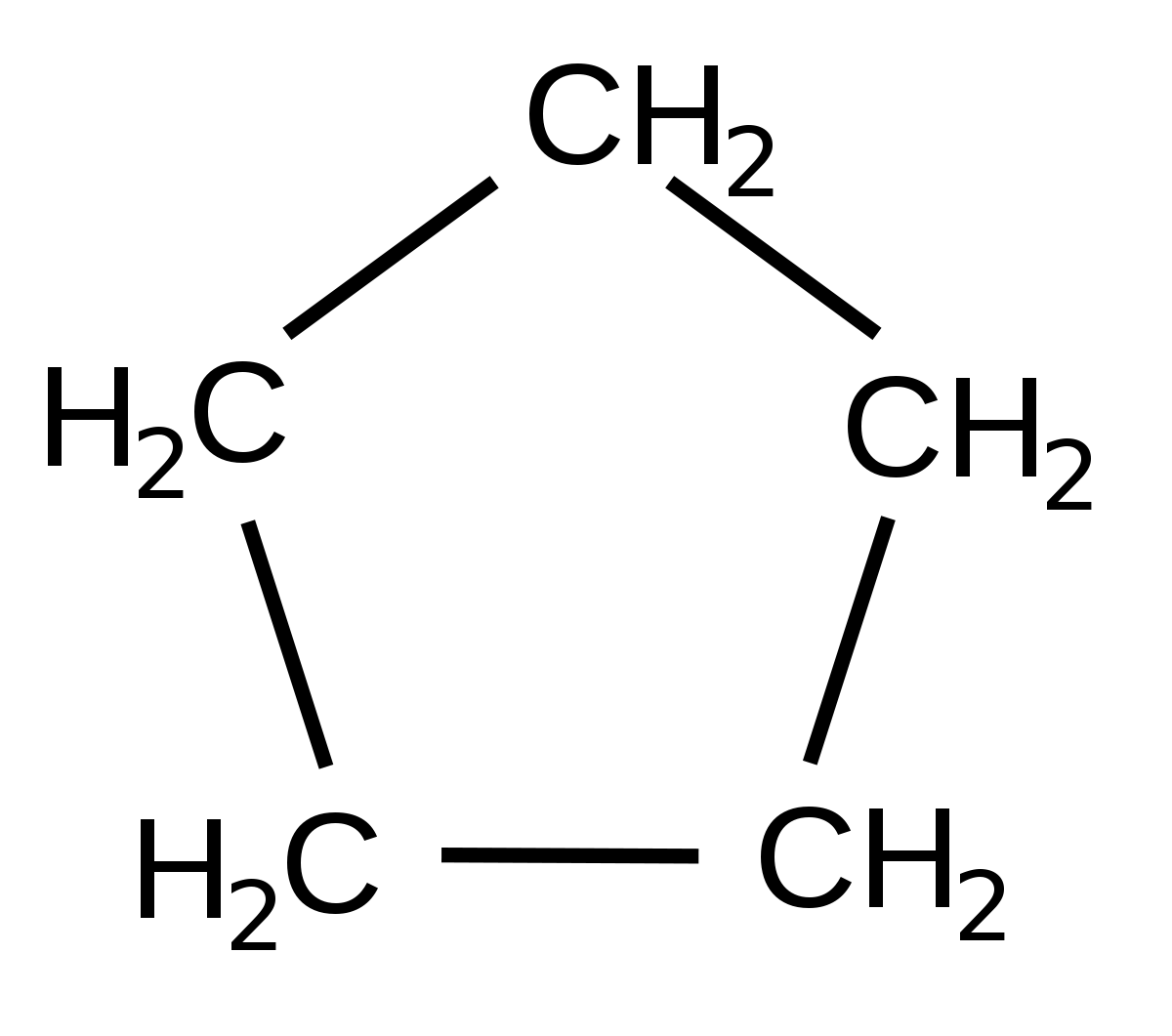
Los hidrocarburos son compuestos formados por carbono e hidrógeno, los mismos pueden tener una estructura lineal, ramificada o presentarse en forma de ciclos. Los hidrocarburos ramificados contienen sustituyentes. Un sustituyente puede ser un átomo diferente al C o al H, un grupo funcional o un grupo alquilo.

La nomenclatura de los compuestos orgánicos se basa en las recomendaciones de la IUPAC (Unión Internacional de Química Pura y Aplicada). Los cuatro alcanos, alquenos y alquinos más sencillos poseen nombres no sistemáticos, para nombrar los siguientes compuestos se hará uso de prefijos griegos.

Tabla 1.
En la siguiente tabla se puede ver la nomenclatura de algunos alcanos, se utilizó “prefijo + terminación ano” dado que dichos compuestos poseen únicamente enlaces simples C-C.
| Nombre del hidrocarburo | Fórmula | Número de átomos de C |
| metano | CH4 | 1 |
| etano | CH3-CH3 | 2 |
| propano | CH3-CH2-CH3 | 3 |
| butano | CH3-(CH2)2-CH3 | 4 |
| pentano | CH3-(CH2)3-CH3 | 5 |
| hexano | CH3-(CH2)4-CH3 | 6 |
| heptano | CH3-(CH2)5-CH3 | 7 |
| octano | CH3-(CH2)6-CH3 | 8 |
| nonano | CH3-(CH2)7-CH3 | 9 |
| decano | CH3-(CH2)8-CH3 | 10 |
Tabla 2.
Cuando existen elementos dentro de un paréntesis en una fórmula química significa que estos se repiten tantas veces como el subíndice fuera del paréntesis lo determine.
CH3–(CH2)4-CH3 = CH3–CH2-CH2-CH2-CH2–CH3
Los nombres de los alquenos y alquinos se construyen del mismo modo que los alcanos expresados en la Tabla 2, con la particularidad de que en alquenos y alquinos pueden existir más de un doble o triple enlace.
EJEMPLO 1: Los tres compuestos que se observan a continuación contienen 2 carbonos en su fórmula, por ello se escriben utilizando el prefijo et-, se diferencian entre sí por sus enlaces, simple, doble y triple respectivamente.
CH3-CH3 CH2=CH2 CH≡CH
etano eteno etino
EJEMPLO 2: Los siguientes compuestos tienen en común que poseen 4 carbonos cada uno, se diferencian en sus terminaciones. En el caso de alquenos y alquinos se indica la posición del doble o triple enlace.
CH3-CH2-CH2-CH3 CH2=CH-CH2-CH3 CH≡C-CH2-CH3
butano 1–buteno 1–butino
EJEMPLO 3: Cuando los dobles o triples enlaces se encuentran más de una vez, en el nombre se agrega un prefijo griego (di, tri, tetra, etc.) que indica la cantidad de dobles o triples enlaces presentes.
CH2=C=CH-CH3
1,2 butadieno

Los prefijos griegos se utilizan con frecuencia en las ciencias exactas y naturales, por ejemplo, en química para nombrar hidrocarburos y en matemática para dar nombre a las figuras geométricas (triángulo, pentágono, etc.).
| 1 | mono- | 8 | octa- | 15 | pentadeca- | ||
| 2 | di- | 9 | nona- | 16 | hexadeca- | ||
| 3 | tri- | 10 | deca- | 17 | heptadeca- | ||
| 4 | tetra- | 11 | undeca- | 18 | octadeca- | ||
| 5 | penta- | 12 | dodeca- | 19 | nonadeca- | ||
| 6 | hexa- | 13 | trideca- | 20 | icosa- | ||
| 7 | hepta- | 14 | tetradeca- | 100 | hecta- |
REGLAS IUPAC
Para poder nombrar hidrocarburos lineales, ramificados o cíclicos es indispensable conocer las reglas de la IUPAC. Como se puede observar en los ejemplos anteriores, nombrar hidrocarburos lineales no es una tarea difícil. Si se desea dar nombre a ramificados, es necesario conocer algunas reglas específicas y tener en cuenta que estos compuestos poseen una cadena principal de átomos de carbono y sustituyentes.
Reemplazan a un hidrógeno de la cadena carbonada y pueden ser:
- Átomos distintos al carbono o al hidrógeno, por ejemplo el Br, Cl, I, etc.
- Grupos funcionales.
- Grupo alquilo
GRUPO ALQUILO: Cuando a un alcano se le quita un hidrógeno se genera un grupo alquilo.
| ALCANO | GRUPO ALQUILO | ||
| metano | CH4 | metilo | -CH3 |
| etano | CH3-CH3 | etilo | -CH2-CH3 |
| propano | CH3-CH2-CH3 | propilo | -CH2-CH2-CH3 |
Cuando el alquilo se une a la cadena principal, se elimina la letra “o” final para nombrar el compuesto, por ejemplo:
-CH3 es un metilo, al ser un sustituyente se nombra como metil:  3-metil-hexano
3-metil-hexano
REGLAS PARA NOMBRAR HIDROCARBUROS RAMIFICADOS
PARA TENER EN CUENTA: La numeración de la cadena inicia en el extremo más cercano al sustituyente.
- Identificar la cadena principal (es la cadena más larga de átomos consecutivos de carbono).
 La cadena más larga de carbonos contiene 6 C.
La cadena más larga de carbonos contiene 6 C.
 En este ejemplo la cadena no está ubicada en forma lineal, cuenta con 6 C.
En este ejemplo la cadena no está ubicada en forma lineal, cuenta con 6 C.
2. Escribir el número que indica la posición de los radicales alquilo y nombrarlos (en orden alfabético si hay más de uno). Se finaliza nombrando la cadena principal.
 3- metil-hexano
3- metil-hexano
En el carbono 3 se encuentra un sustituyente (metil), por ello el se escribe: 3-metil.
Como la cadena principal contiene 6 C, corresponde a un hexano, por ello el nombre es: 3-metil hexano.
 5-etil-3-metil-octano
5-etil-3-metil-octano
En el carbono 3 se observa un sustituyente metil y en la posición del carbono 5 la ramificación es un etil. Como deben escribirse en orden alfabético queda: 5-etil-3-metil.
La cadena principal contiene 8 C y todos los enlaces son simples, por lo tanto el compuesto es: 5-etil-3-metil-octano.
3. Si en la cadena los sustituyentes son halógenos (elementos del grupo VII de la tabla periódica) y además de estos hay alquilos, se nombra primero a los halógenos.
 2-cloro-3-metil-hexano
2-cloro-3-metil-hexano
4. Si el radical se repite se utilizan los prefijos di, tri, tetra, etc.
 3,5-dimetil octano
3,5-dimetil octano
5. Los dobles y triples enlaces de deben nombrar después de los sustituyentes.
 3-metil-1-octeno
3-metil-1-octeno
En el ejemplo se comienza a numerar la cadena principal a partir del extremo más cercano al doble enlace y luego se nombra primero la posición y el tipo de radical (3-metil), finalizando con la ubicación del doble enlace y el alqueno de 8 carbonos (1-octeno).
A PRACTICAR LO APRENDIDO
- Formular los siguientes compuestos:
a) 2,3-dimetil-pentano
b) 3-etil-4-metil-1-hexeno
c) 4-metil-1,6-octadiino
2. Nombrar los siguientes compuestos:
a) ![]()
b) ![]()
c) ![]()
respuestas
1.
a)
b) 
c) ![]()
2.
a) 2,3,5-trimetil-heptano
b) 2-metil-2,4-heptadieno
c) 4-metil-2-hexino




 VOLVER A LOS ARTÍCULOS
VOLVER A LOS ARTÍCULOS






 1- penteno
1- penteno 1-penteno
1-penteno